Công thức cấu tạo C3H4 đại diện cho một nhóm các hợp chất hydrocarbon không no với ba nguyên tử carbon và bốn nguyên tử hydro. Sự đa dạng trong cách sắp xếp liên kết hóa học đã tạo nên các đồng phân thú vị, mỗi loại mang những đặc tính và ứng dụng riêng biệt trong lĩnh vực hóa học hữu cơ. Việc tìm hiểu chi tiết về cấu trúc, tính chất và sự khác biệt giữa các đồng phân này không chỉ củng cố kiến thức nền tảng mà còn mở ra cánh cửa đến những ứng dụng thực tiễn của chúng. Bài viết này sẽ đi sâu phân tích từng loại đồng phân, giúp người đọc nắm vững khái niệm và ý nghĩa của công thức C3H4.
C3H4 là gì? Tổng quan về hợp chất hydrocarbon không no
Trong hóa học hữu cơ, C3H4 thuộc nhóm hydrocarbon không no, tức là các hợp chất chỉ chứa carbon và hydro nhưng có ít nhất một liên kết bội (liên kết đôi hoặc liên kết ba) giữa các nguyên tử carbon. Công thức tổng quát của ankadien và ankin (hai loại hydrocarbon không no phổ biến) là CnH2n-2, và C3H4 hoàn toàn phù hợp với công thức này khi n = 3 (3 2 – 2 = 4). Điều này cho thấy C3H4 có thể là một ankin (chứa một liên kết ba) hoặc một ankadien (chứa hai liên kết đôi). Sự tồn tại của các liên kết bội mang lại cho những hợp chất này khả năng tham gia vào nhiều phản ứng hóa học đặc trưng, đặc biệt là phản ứng cộng, điều này là nền tảng cho nhiều quá trình tổng hợp quan trọng trong công nghiệp và nghiên cứu.
Hydrocarbon không no đóng vai trò thiết yếu trong ngành hóa dầu, dược phẩm và vật liệu polymer. Việc hiểu rõ về cấu trúc và tính chất của chúng là bước đầu tiên để khai thác tiềm năng ứng dụng. Trong trường hợp của C3H4, số lượng nguyên tử carbon nhỏ (chỉ 3) giới hạn số lượng các cấu trúc có thể có nhưng lại làm cho mỗi đồng phân trở nên đặc biệt và dễ phân biệt. Mỗi đồng phân sẽ có một cách sắp xếp liên kết khác nhau, dẫn đến hình dạng phân tử và tính chất hóa học riêng biệt.
Các đồng phân cấu tạo của C3H4
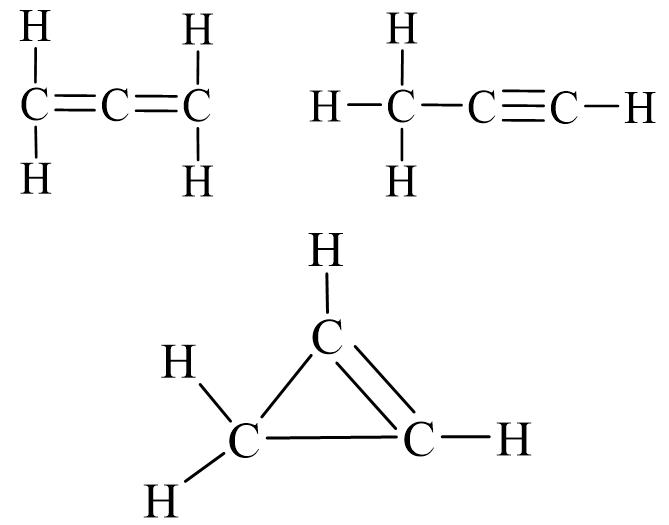
Khi nói đến công thức cấu tạo C3H4, chúng ta đang nói về một số đồng phân cấu tạo khác nhau. Đồng phân là các hợp chất có cùng công thức phân tử nhưng có cấu trúc và cách sắp xếp nguyên tử khác nhau, dẫn đến các tính chất vật lý và hóa học khác nhau. Đối với C3H4, các đồng phân chính bao gồm một ankin và một ankadien, cùng với một đồng phân vòng ít phổ biến hơn. Mỗi cấu trúc này mang đến một bức tranh độc đáo về liên kết và hình học phân tử.
Propin (Methylaxetilen)
Propin, hay còn gọi là methylaxetilen, là một trong những đồng phân quan trọng nhất của C3H4. Cấu trúc của propin được đặc trưng bởi một liên kết ba giữa hai nguyên tử carbon, với một nhóm methyl (-CH3) gắn vào một trong hai carbon liên kết ba. Cụ thể, công thức cấu tạo của propin là CH≡C-CH3.
Liên kết ba carbon-carbon là một liên kết rất mạnh, được hình thành từ một liên kết sigma và hai liên kết pi. Sự hiện diện của liên kết ba này làm cho các nguyên tử carbon tham gia liên kết có trạng thái lai hóa sp, dẫn đến hình học phân tử tuyến tính xung quanh liên kết ba. Điều này có nghĩa là các nguyên tử carbon và hydro liền kề với liên kết ba nằm trên một đường thẳng. Liên kết ba mang lại cho propin khả năng phản ứng cộng rất mạnh với các tác nhân như hydro, halogen, hoặc hydro halogenua.
Một đặc điểm nổi bật khác của propin là sự hiện diện của nguyên tử hydro linh động gắn vào carbon có liên kết ba đầu mạch (nếu có, nhưng trong propin thì không có H đầu mạch). Tuy nhiên, nếu là một ankin có liên kết ba ở vị trí đầu mạch (ví dụ axetilen, C2H2), hydro gắn vào carbon sp sẽ có tính axit yếu và có thể bị thay thế bởi kim loại kiềm hoặc ion kim loại chuyển tiếp như bạc. Propin không có hydro đầu mạch linh động như axetilen, nên nó không phản ứng với dung dịch AgNO3/NH3 để tạo kết tủa. Propin là một khí không màu ở nhiệt độ phòng, dễ cháy và thường được sử dụng trong tổng hợp hữu cơ.
Propa-1,2-dien (Allen)
Đồng phân thứ hai của C3H4 là propa-1,2-dien, thường được biết đến với tên gọi ngắn gọn là Allen. Cấu trúc của Allen khác biệt hoàn toàn so với propin, với hai liên kết đôi liền kề nhau trong chuỗi carbon. Công thức cấu tạo của Allen là CH2=C=CH2. Trong cấu trúc này, carbon trung tâm tham gia vào hai liên kết đôi, mỗi liên kết với một trong hai carbon đầu mạch.
Liên kết đôi carbon-carbon bao gồm một liên kết sigma và một liên kết pi. Carbon trung tâm trong Allen có trạng thái lai hóa sp, trong khi hai carbon đầu mạch có trạng thái lai hóa sp2. Điều đặc biệt về cấu trúc của Allen là hai liên kết đôi này nằm trong các mặt phẳng vuông góc với nhau. Cụ thể, nhóm CH2 ở một đầu nằm trong một mặt phẳng, trong khi nhóm CH2 ở đầu kia nằm trong mặt phẳng vuông góc với mặt phẳng thứ nhất. Sự sắp xếp hình học này tạo nên một cấu trúc không phẳng và có tính chất đặc biệt.
Giống như propin, Allen cũng là một hydrocarbon không no và có khả năng tham gia vào các phản ứng cộng. Tuy nhiên, do có hai liên kết đôi thay vì một liên kết ba, Allen có xu hướng phản ứng theo cách khác và có độ bền nhiệt động học kém hơn propin. Allen cũng là một khí không màu, dễ cháy và được sử dụng trong một số tổng hợp hữu cơ chuyên biệt. Các hợp chất diene có liên kết đôi liền kề (cumulated dienes) như Allen thường có tính chất hóa học riêng biệt do cấu trúc đặc thù của chúng.
Xicloanken vòng 3 cạnh có một liên kết đôi (Cyclopropene)
Ngoài hai đồng phân mạch hở là propin và Allen, công thức cấu tạo C3H4 còn có thể tồn tại dưới dạng đồng phân mạch vòng, đó là cyclopropene. Cyclopropene là một hợp chất hydrocarbon vòng ba cạnh, trong đó có một liên kết đôi carbon-carbon. Cấu trúc của nó là một tam giác, với hai carbon tham gia liên kết đôi và một carbon bão hòa còn lại.
Tuy nhiên, cyclopropene là một hợp chất rất không bền vững. Nguyên nhân chính là do sự căng vòng (ring strain) cực lớn. Góc liên kết trong một vòng ba cạnh lý tưởng là 60 độ, nhưng đối với carbon lai hóa sp2 (tham gia liên kết đôi), góc liên kết lý tưởng là khoảng 120 độ. Sự khác biệt lớn này tạo ra một lực căng đáng kể trong phân tử, làm cho cyclopropene trở nên rất kém bền và dễ bị phá vỡ. Nó thường chỉ tồn tại trong điều kiện thí nghiệm đặc biệt và không phải là một đồng phân phổ biến hay ổn định như propin hay Allen trong các điều kiện thông thường.
Trong phạm vi kiến thức phổ thông, khi nhắc đến các đồng phân của C3H4, người ta thường tập trung vào propin và Allen vì chúng là những hợp chất ổn định hơn và có ý nghĩa thực tiễn rõ rệt hơn. Cyclopropene chủ yếu được nghiên cứu trong các lĩnh vực hóa học hữu cơ nâng cao để hiểu về các nguyên lý cấu trúc và độ bền phân tử.
Đặc điểm chung về tính chất hóa học của C3H4
Các đồng phân của công thức cấu tạo C3H4, bao gồm propin và Allen, đều là hydrocarbon không no, do đó chúng có những tính chất hóa học đặc trưng của các hợp chất chứa liên kết bội. Những tính chất này là cơ sở cho nhiều phản ứng quan trọng trong tổng hợp hóa học.
Phản ứng cộng Hydro (Hydrogenation)
Cả propin và Allen đều có thể tham gia phản ứng cộng hydro (H2) dưới điều kiện thích hợp (xúc tác Ni, Pt hoặc Pd) và nhiệt độ. Phản ứng này phá vỡ các liên kết pi, chuyển đổi hydrocarbon không no thành hydrocarbon no.
- Propin (CH≡C-CH3) sẽ cộng 2 phân tử H2 để tạo thành propan (CH3-CH2-CH3). Nếu xúc tác là Pd/PbCO3 (xúc tác Lindlar) hoặc Ni/B (xúc tác P-2), phản ứng có thể dừng lại ở alkene là propene (CH2=CH-CH3).
- Allen (CH2=C=CH2) cũng sẽ cộng 2 phân tử H2 để tạo thành propan (CH3-CH2-CH3).
Phản ứng cộng Halogen (Halogenation)
Cả hai đồng phân đều phản ứng mạnh với các halogen như clo (Cl2) và brom (Br2) ở nhiệt độ phòng, làm mất màu dung dịch brom. Phản ứng này được dùng để nhận biết sự có mặt của liên kết bội.
- Propin (CH≡C-CH3) sẽ cộng 2 phân tử Br2, tạo thành 1,1,2,2-tetrabromopropan.
- Allen (CH2=C=CH2) cũng sẽ cộng 2 phân tử Br2, tạo thành 1,1,2,2-tetrabromopropan, hoặc 1,2,2,3-tetrabromopropan tùy vào vị trí cộng.
Phản ứng cộng Hydro Halogenua (Hydrohalogenation)
Propin và Allen cũng có thể cộng các hợp chất hydro halogenua (HX, ví dụ HCl, HBr). Phản ứng này thường tuân theo quy tắc Markovnikov, trong đó nguyên tử hydro sẽ gắn vào carbon có nhiều hydro hơn (hoặc ít nhóm thế hơn) trong liên kết bội, và halogen gắn vào carbon còn lại.
- Propin (CH≡C-CH3) cộng HCl sẽ tạo ra 2-cloropropen, sau đó có thể cộng thêm HCl tạo ra 2,2-dicloropropan.
- Allen (CH2=C=CH2) khi cộng HCl sẽ tạo ra 2-cloropropen, sau đó có thể cộng thêm HCl tương tự propin.
Phản ứng trùng hợp (Polymerization)
Dưới các điều kiện thích hợp (xúc tác, nhiệt độ, áp suất), các hydrocarbon không no có thể trùng hợp để tạo thành các polymer có mạch dài. Propin và Allen cũng có khả năng tham gia vào phản ứng này, tạo ra các vật liệu polymer với cấu trúc và tính chất đặc biệt. Ví dụ, propin có thể trùng hợp thành polypropyne.
Phản ứng cháy
Giống như tất cả các hydrocarbon, propin và Allen đều dễ cháy trong không khí hoặc oxy, tạo ra carbon dioxide (CO2) và nước (H2O), kèm theo việc giải phóng một lượng lớn nhiệt năng. C3H4 + 4O2 → 3CO2 + 2H2O
Phản ứng với dung dịch AgNO3/NH3 (Chỉ đối với ankin có H linh động)
Đây là một tính chất hóa học quan trọng để phân biệt giữa các loại ankin.
- Propin (CH≡C-CH3) không có nguyên tử hydro linh động gắn trực tiếp vào carbon có liên kết ba đầu mạch. Do đó, propin không phản ứng với dung dịch bạc nitrat trong amoniac (AgNO3/NH3) để tạo kết tủa. Điều này giúp phân biệt propin với các ankin đầu mạch như axetilen.
- Allen (CH2=C=CH2) là một ankadien, không có liên kết ba và do đó cũng không có hydro linh động. Vì vậy, Allen cũng không phản ứng với dung dịch AgNO3/NH3.
Những phản ứng này là cơ sở để nhận biết, phân loại và tổng hợp các hợp chất hữu cơ, cho thấy sự linh hoạt trong hóa học của các đồng phân C3H4.
So sánh Propin và Allen: Điểm giống và khác biệt
Mặc dù cùng có công thức cấu tạo C3H4, propin và Allen là hai đồng phân có cấu trúc và tính chất hóa học khác nhau rõ rệt. Việc so sánh chúng giúp làm nổi bật những đặc điểm riêng biệt của từng loại.
Điểm giống nhau:
- Công thức phân tử: Cả hai đều có công thức phân tử C3H4, thuộc nhóm hydrocarbon không no.
- Phản ứng cộng: Cả propin và Allen đều có khả năng tham gia phản ứng cộng với H2, X2 (halogen), và HX (hydro halogenua) do sự hiện diện của các liên kết pi.
- Phản ứng cháy: Đều cháy tỏa nhiệt, tạo ra CO2 và H2O.
- Trạng thái vật lý: Ở điều kiện thường, cả hai đều là chất khí không màu.
- Sử dụng trong tổng hợp: Cả hai đều được sử dụng làm nguyên liệu trong các phản ứng tổng hợp hữu cơ.
Điểm khác biệt:
Đặc điểm Propin (Methylaxetilen) Allen (Propa-1,2-dien) Cấu trúc CH≡C-CH3 (một liên kết ba) CH2=C=CH2 (hai liên kết đôi liền kề) Lai hóa Carbon liên kết ba: sp; Carbon methyl: sp3 Carbon trung tâm: sp; Carbon đầu mạch: sp2 Hình học Phần liên kết ba: thẳng; Tổng thể: gần tuyến tính Các nhóm CH2 ở hai đầu nằm trong hai mặt phẳng vuông góc Tính chất hóa học Phản ứng AgNO3/NH3 Không phản ứng (không có H linh động đầu mạch) Không phản ứng (không có liên kết ba đầu mạch) Độ bền Bền hơn Allen về mặt nhiệt động học. Kém bền hơn propin. Phản ứng đặc trưng Phản ứng của ankin, có thể dừng ở alkene khi hydro hóa. Phản ứng của diene với liên kết đôi liền kề.
Sự khác biệt về cấu trúc liên kết và hình học phân tử là nguyên nhân chính dẫn đến sự khác biệt về tính chất hóa học giữa propin và Allen. Liên kết ba trong propin mang lại khả năng phản ứng cộng hai giai đoạn và sự khác biệt về tính axit của hydro. Trong khi đó, hai liên kết đôi liền kề của Allen tạo ra một cấu hình không phẳng độc đáo và có thể ảnh hưởng đến cơ chế phản ứng của nó. Việc nắm rõ những điểm khác biệt này là cực kỳ quan trọng để hiểu sâu hơn về hóa học hữu cơ và ứng dụng thực tiễn của các hợp chất này. Để hiểu rõ hơn về các khái niệm hóa học cơ bản và nâng cao, bạn có thể tham khảo thêm tại lophoctichcuc.com.
Phương pháp điều chế C3H4 và các ứng dụng quan trọng
Các đồng phân của công thức cấu tạo C3H4 không chỉ là đối tượng nghiên cứu hấp dẫn mà còn có những ứng dụng thực tiễn nhất định, đòi hỏi các phương pháp điều chế đặc thù.
Điều chế Propin (Methylaxetilen)
Propin thường được điều chế thông qua các phản ứng loại bỏ hoặc từ các ankin đơn giản hơn:
- Từ 1,2-dibromopropan hoặc 1,1-dibromopropan: Phản ứng loại bỏ hai phân tử HBr từ dẫn xuất dibromo của propan bằng dung dịch kiềm mạnh như KOH trong etanol ở nhiệt độ cao.
- CH2Br-CHBr-CH3 + 2KOH (ancol, nhiệt) → CH≡C-CH3 + 2KBr + 2H2O
- CH3-CBr2-CH3 + 2KOH (ancol, nhiệt) → CH≡C-CH3 + 2KBr + 2H2O
- Tổng hợp từ axetilen: Propin có thể được điều chế bằng cách cho axetilen phản ứng với một tác nhân kim loại kiềm để tạo ra axetilua kim loại, sau đó phản ứng với metyl halogenua.
- HC≡CH + Na → HC≡CNa + 1/2 H2
- HC≡CNa + CH3Br → HC≡C-CH3 + NaBr
Điều chế Allen (Propa-1,2-dien)
Việc điều chế Allen đòi hỏi các phương pháp chuyên biệt hơn do cấu trúc liên kết đôi liền kề của nó:
- Từ 2,3-dibromopropene: Loại bỏ HBr bằng kiềm mạnh.
- CH2=CBr-CH2Br + 2KOH (ancol, nhiệt) → CH2=C=CH2 + 2KBr + 2H2O
- Phân hủy nhiệt của các hợp chất vòng: Một số hợp chất vòng đặc biệt có thể bị phân hủy nhiệt để tạo ra Allen.
Ứng dụng của các đồng phân C3H4
Propin và Allen, mặc dù không được sử dụng rộng rãi như ethylene hay acetylene, vẫn có vai trò quan trọng trong một số lĩnh vực:
- Nguyên liệu tổng hợp hữu cơ: Cả hai đều là các đơn vị cấu trúc hữu ích trong tổng hợp các hợp chất hữu cơ phức tạp hơn. Chúng có thể được dùng để điều chế các dẫn xuất halogen, các loại rượu, hoặc các hợp chất vòng.
- Nhiên liệu: Propin có thể được sử dụng làm nhiên liệu trong một số ứng dụng chuyên biệt, đặc biệt là khi cần ngọn lửa có nhiệt độ cao.
- Nghiên cứu khoa học: Các đồng phân này là đối tượng nghiên cứu quan trọng trong hóa học vật lý hữu cơ để hiểu về tính chất của liên kết bội, độ bền phân tử, và cơ chế phản ứng. Chúng cung cấp các mô hình lý tưởng để nghiên cứu sự chuyển đổi giữa các trạng thái lai hóa của carbon.
- Sản xuất vật liệu: Trong một số trường hợp, các dẫn xuất của propin và Allen có thể được dùng làm monome trong sản xuất polymer chuyên dụng, tạo ra vật liệu có tính chất độc đáo.
Các khái niệm liên quan đến đồng phân cấu tạo C3H4 cần nắm vững
Để hiểu sâu sắc về công thức cấu tạo C3H4 và các đồng phân của nó, việc nắm vững một số khái niệm cơ bản trong hóa học hữu cơ là điều cần thiết. Những khái niệm này tạo nền tảng cho việc phân tích và dự đoán tính chất của các hợp chất hydrocarbon không no.
- Đồng phân: Khái niệm cốt lõi cho việc nghiên cứu C3H4. Đồng phân là các hợp chất có cùng công thức phân tử nhưng có cấu trúc hoặc cách sắp xếp không gian của các nguyên tử khác nhau. Đối với C3H4, chúng ta có đồng phân cấu tạo như propin và Allen, thể hiện sự khác biệt trong thứ tự liên kết.
- Hydrocarbon không no: Là các hợp chất hữu cơ chỉ chứa carbon và hydro, có chứa ít nhất một liên kết bội (liên kết đôi C=C hoặc liên kết ba C≡C). Các liên kết bội này là tâm điểm của nhiều phản ứng hóa học quan trọng.
- Phản ứng cộng: Là phản ứng đặc trưng của các hydrocarbon không no, trong đó các phân tử nhỏ (như H2, X2, HX) thêm vào liên kết bội, phá vỡ liên kết pi và tạo thành liên kết sigma. Đây là cách để chuyển hóa các hợp chất không no thành các hợp chất bão hòa hoặc có độ không no thấp hơn.
- Phản ứng thế H linh động (đối với ankin): Đối với các ankin có liên kết ba ở đầu mạch (R-C≡CH), nguyên tử hydro gắn với carbon mang liên kết ba có tính axit yếu và có thể bị thay thế bởi các ion kim loại nặng như Ag+ (trong dung dịch AgNO3/NH3) để tạo kết tủa. Propin (CH3-C≡CH) không có tính chất này vì không có H linh động ở đầu mạch.
- Quy tắc Markovnikov: Một quy tắc quan trọng áp dụng cho phản ứng cộng của HX vào alkene hoặc alkyne không đối xứng. Theo quy tắc này, nguyên tử hydro (từ HX) sẽ ưu tiên cộng vào carbon của liên kết bội có nhiều nguyên tử hydro hơn (hoặc ít nhóm thế hơn), trong khi phần còn lại của HX (X) sẽ cộng vào carbon còn lại.
- Lai hóa: Khái niệm về lai hóa quỹ đạo nguyên tử (sp, sp2, sp3) giúp giải thích hình học phân tử và góc liên kết của các nguyên tử carbon trong các hợp chất hữu cơ. Carbon trong liên kết ba có lai hóa sp (góc 180°), carbon trong liên kết đôi có lai hóa sp2 (góc 120°), và carbon trong liên kết đơn có lai hóa sp3 (góc 109.5°). Việc hiểu rõ lai hóa sẽ làm sáng tỏ cấu trúc không gian của propin và Allen.
- Căng vòng (Ring Strain): Là hiện tượng xảy ra trong các hợp chất vòng nhỏ (như cyclopropene). Các góc liên kết trong vòng bị buộc phải lệch khỏi góc lý tưởng của trạng thái lai hóa, gây ra lực căng trong phân tử và làm giảm độ bền của hợp chất. Đây là lý do cyclopropene rất không bền.
Nắm vững các thuật ngữ và nguyên lý này sẽ giúp bạn không chỉ giải thích được sự đa dạng của công thức cấu tạo C3H4 mà còn áp dụng kiến thức này vào việc giải quyết các bài tập hóa học và hiểu các phản ứng phức tạp hơn.
Câu hỏi thường gặp về công thức cấu tạo C3H4
Khi tìm hiểu về công thức cấu tạo C3H4, người học thường có một số thắc mắc phổ biến. Dưới đây là những câu hỏi thường gặp cùng với lời giải đáp chi tiết, giúp củng cố kiến thức và làm rõ các điểm còn băn khoăn.
C3H4 là ankin hay ankadien?
C3H4 có thể là cả ankin và ankadien.
- Ankin: Là các hydrocarbon không no có một liên kết ba carbon-carbon. Đồng phân propin (CH≡C-CH3) của C3H4 là một ankin.
- Ankadien: Là các hydrocarbon không no có hai liên kết đôi carbon-carbon. Đồng phân propa-1,2-dien (Allen, CH2=C=CH2) của C3H4 là một ankadien. Tùy thuộc vào cách sắp xếp liên kết mà C3H4 có thể thuộc một trong hai nhóm này.
C3H4 có bao nhiêu đồng phân?
Về mặt lý thuyết, C3H4 có ba đồng phân cấu tạo chính:
- Propin (Methylaxetilen): CH≡C-CH3 (ankin)
- Propa-1,2-dien (Allen): CH2=C=CH2 (ankaduen có liên kết đôi liền kề)
- Cyclopropene: Một vòng 3 carbon với một liên kết đôi (anken vòng, rất kém bền). Trong chương trình phổ thông và ứng dụng thực tế phổ biến, thường chỉ xét đến propin và Allen do tính ổn định và phổ biến của chúng.
Propin có tác dụng với AgNO3/NH3 không? Tại sao?
Không, propin (CH3-C≡CH) không phản ứng với dung dịch bạc nitrat trong amoniac (AgNO3/NH3) để tạo kết tủa. Lý do là vì chỉ những ankin có liên kết ba ở vị trí đầu mạch (R-C≡CH) mới có nguyên tử hydro linh động gắn trực tiếp vào carbon mang liên kết ba. Nguyên tử hydro này có tính axit yếu và có thể bị thay thế bởi ion Ag+ để tạo thành kết tủa bạc axetylua. Propin có công thức CH3-C≡CH, trong đó carbon mang liên kết ba không có hydro linh động.
Allen có phản ứng với AgNO3/NH3 không? Tại sao?
Không, Allen (CH2=C=CH2) không phản ứng với dung dịch AgNO3/NH3. Lý do là vì Allen là một diene (có hai liên kết đôi), không phải là ankin. Phản ứng với dung dịch AgNO3/NH3 chỉ xảy ra với ankin có liên kết ba đầu mạch (R-C≡CH).
Độ bền của propin và allen?
Propin thường được coi là bền hơn Allen về mặt nhiệt động học.
- Propin có một liên kết ba mạnh và cấu trúc thẳng ở phần liên kết bội, ít căng thẳng.
- Allen có hai liên kết đôi liền kề tạo ra một cấu hình không phẳng và sự tương tác giữa các electron pi có thể làm giảm độ bền của nó so với propin. Thêm vào đó, năng lượng căng của các liên kết đôi kề nhau cũng góp phần làm nó kém bền hơn.
Phản ứng đặc trưng của C3H4 là gì?
Phản ứng đặc trưng nhất của các đồng phân C3H4 (propin và Allen) là phản ứng cộng. Cả hai đều có khả năng cộng hydro (H2), halogen (X2 như Br2, Cl2) và hydro halogenua (HX như HCl, HBr) vào các liên kết bội của chúng. Ngoài ra, chúng còn tham gia phản ứng cháy. Đối với propin, không có phản ứng thế H linh động như các ankin đầu mạch.
Những câu hỏi và trả lời này hy vọng sẽ giúp bạn có cái nhìn toàn diện và rõ ràng hơn về công thức cấu tạo C3H4 và các đồng phân của nó. Việc hiểu rõ những điểm này là chìa khóa để tiến xa hơn trong việc nghiên cứu hóa học hữu cơ.
Các đồng phân của công thức cấu tạo C3H4 – propin và Allen – là những hợp chất hydrocarbon không no tiêu biểu, mỗi loại mang trong mình một cấu trúc phân tử và bộ tính chất hóa học độc đáo. Propin với liên kết ba và Allen với hai liên kết đôi liền kề, cùng với cyclopropene kém bền, đều đóng góp vào sự phong phú của hóa học hữu cơ. Việc nghiên cứu sâu về các yếu tố như lai hóa, hình học phân tử và cơ chế phản ứng giúp chúng ta không chỉ hiểu rõ bản chất của từng đồng phân mà còn nắm bắt được tầm quan trọng của chúng trong tổng hợp hóa học và nghiên cứu khoa học. Sự khác biệt về tính chất hóa học giữa chúng là bằng chứng rõ ràng nhất cho thấy cùng một công thức phân tử có thể tạo ra những chất có đặc điểm hoàn toàn riêng biệt.

