Đề bài
Câu 1 :
Số electron ở lớp ngoài cùng của mỗi nguyên tử nguyên tố halogen là
-
A.
5
-
B.
7
-
C.
2
-
D.
8
Câu 2 :
Tính chất hóa học đặc trưng của các đơn chất halogen là
-
A.
tính khử
-
B.
tính base
-
C.
tính acid
-
D.
tính oxi hóa
Câu 3 :
Trong tự nhiên, nguyên tố fluorine tồn tại phổ biến nhất ở dạng hợp chất là
-
A.
Na3AlF6
-
B.
NaF
-
C.
HF
-
D.
CaF2
Câu 4 :
Ở điều kiện thường, halogen tồn tại ở thể rắn, có màu đen tím là
-
A.
F2
-
B.
Cl2
-
C.
Br2
-
D.
I2
Câu 5 :
Đặc điểm nào dưới đây không phải là đặc điểm chung của các nguyên tố halogen (F, Cl, Br, I)?
-
A.
Nguyên tử có khả năng thu thêm 1e.
-
B.
Tạo ra hợp chất liên kết cộng hóa trị có cực với hiđro.
-
C.
Có số oxi hóa -1 trong mọi trường hợp.
-
D.
Lớp electron ngoài cùng của nguyên tử có 7 electron.
Câu 6 :
Đặc điểm nào dưới đây là đặc điểm chung của các đơn chất halogen (F2, Cl2, Br2, I2)?
-
A.
Ở điều kiện thường là các chất khí.
-
B.
Có tính oxi hóa mạnh.
-
C.
Vừa có tính oxi hóa, vừa có tính khử.
-
D.
Tác dụng mạnh với nước.
Câu 7 :
Các nguyên tố halogen thuộc nhóm nào trong bảng tuần hoàn
-
A.
VIIIA
-
B.
VIA
-
C.
VIIA
-
D.
IIA
Câu 8 :
Trong cơ thể người, nguyên tố iodine tập trung ở tuyến nào sau đây?
-
A.
Tuyến thượng thận
-
B.
Tuyến tụy
-
C.
Tuyến yên
-
D.
Tuyến giáp trạng
Câu 9 :
Trong dãy halogen, nguyên tử có độ âm điện nhỏ nhất là
-
A.
fluorine
-
B.
chlorine
-
C.
bromine
-
D.
iodine
Câu 10 :
Chỉ thị nào sau đây thường dùng để nhận biết dung dịch I2
-
A.
Phenolphtalein
-
B.
Hồ tinh bột
-
C.
Quỳ tím
-
D.
Nước vôi trong
Câu 11 :
Phát biểu nào sau đây không đúng khi nói về nguyên tử các nguyên tố nhóm VIIA?
-
A.
Có 7 electron hóa trị.
-
B.
Theo chiều tăng dần của điện tích hạt nhân nguyên tử thì độ âm điện giảm.
-
C.
Theo chiều tăng dần điện tích hạt nhân nguyên tử thì khả năng hút cặp electron liên kết giảm.
-
D.
Theo chiều tăng dần điện tích hạt nhân nguyên tử thì bán kính nguyên tử giảm.
Câu 12 :
Nguyên nhân dẫn đến nhiệt độ nóng chảy, nhiệt độ sôi của các đơn chất halogen tăng từ fluorine đến iodine là do từ fluorine đến iodine,
-
A.
khối lượng phân tử và tương tác van der Waals đều tăng.
-
B.
tính phi kim giảm và tương tác van der Waals tăng.
-
C.
khối lượng phân tử tăng và tương tác van der Waals giảm.
-
D.
độ âm điện và tương tác van der Waals đều giảm.
Câu 13 :
Phát biểu nào sau đây là không đúng khi nói về đơn chất nhóm VIIA?
-
A.
Tính chất đặc trưng là tính oxi hoá.
-
B.
Màu sắc đậm dần từ fluorine đến iodine.
-
C.
Từ fluorine đến bromine rồi iodine, trạng thái của các đơn chất chuyển từ khí đến lỏng rồi rắn.
-
D.
Khả năng phản ứng với nước tăng từ fluorine đến iodine.
Câu 14 :
Phát biểu nào sau đây là SAI khi nói về tính chất và phản ứng của đơn chất nhóm VIIA?
-
A.
Tính oxi hoá giảm dần từ fluorine đến iodine.
-
B.
Phản ứng với nhiều kim loại, tạo thành hợp chất ion. Phản ứng với một số phi kim, tạo thành hợp chất cộng hoá trị.
-
C.
Khi phản ứng với đơn chất hydrogen, các đơn chất nhóm VIIA thể hiện tính khử.
-
D.
Khi phản ứng với đơn chất hydrogen, mức độ phản ứng giảm dần từ fluorine đến iodine.
Câu 15 :
Phát biểu nào sau đây là sai khi nói về phản ứng của đơn chất halogen với hydrogen?
-
A.
Các phản ứng đều phát nhiệt mạnh và kèm hiện tượng nổ.
-
B.
Phản ứng giữa fluorine với hydrogen diễn ra mãnh liệt nhất.
-
C.
Điều kiện và mức độ phản ứng phù hợp với xu hướng giảm dần tính oxi hóa từ fluorine đến iodine.
-
D.
Do hợp chất hydrogen iodide sinh ra kém bền (giá trị năng lượng liên kết nhỏ) nên phản ứng giữa iodine với hydrogen là phản ứng hai chiều.
Câu 16 :
Phát biểu nào sau đây là không đúng khi nói về phản ứng của đơn chất nhóm VIIA với dung dịch muối halide?
-
A.
Bromine phản ứng dễ dàng với dung dịch sodium fluoride để tạo ra đơn chất fluorine.
-
B.
Khi cho vào dung dịch sodium chloride, fluorine sẽ ưu tiên phản ứng với nước.
-
C.
Có thể sục khí chlorine vào dung dịch chứa potassium iodide để thu được iodine.
-
D.
Iodine khó tan trong dung dịch sodium chloride.
Câu 17 :
Phát biểu nào sau đây là không đúng khi nói về một số ứng dụng của đơn chất chlorine?
-
A.
Khí chlorine có thể được dùng để tạo môi trường sát khuẩn cho nguồn nước cấp.
-
B.
Khí chlorine phản ứng với dung dịch sodium hydroxide tạo dung dịch nước Javel dùng để sát khuẩn trong công nghiệp và trong gia đình.
-
C.
Khí chlorine được sử dụng để sản xuất hydrogen chloride, từ đó tạo hydrochloric acid.
-
D.
Do có độc tính, khí chlorine được sử dụng để trừ sâu trong nông nghiệp.
Câu 18 :
Ứng dụng nào sau đây không phải của Cl2?
-
A.
Xử lí nước bể bơi.
-
B.
Sát trùng vết thương trong y tế.
-
C.
Sản xuất nhựa PVC.
-
D.
Sản xuất bột tẩy trắng.
Câu 19 :
Halogen nào được dùng trong sản xuất nhựa Teflon?
-
A.
Chlorine.
-
B.
Iodine.
-
C.
Fluorine.
-
D.
Bromine.
Câu 20 :
Nguyên tố halogen được dùng trong sản xuất nhựa PVC là
-
A.
chlorine.
-
B.
bromine.
-
C.
phosphorus.
-
D.
carbon.
Câu 21 :
Halogen được điều chế bằng cách điện phân có màng ngăn dung dịch muối ăn là
-
A.
fluorine.
-
B.
chlorine.
-
C.
bromine.
-
D.
iodine.
Lời giải và đáp án
Câu 1 :
Số electron ở lớp ngoài cùng của mỗi nguyên tử nguyên tố halogen là
-
A.
5
-
B.
7
-
C.
2
-
D.
8
Đáp án : B
Nguyên tố nhóm halogen nằm ở nhóm VIIA
Nguyên tố nhóm halogen nằm ở nhóm VIIA trong bảng tuần hoàn
=> Có 7 electron ở lớp ngoài cùng
Câu 2 :
Tính chất hóa học đặc trưng của các đơn chất halogen là
-
A.
tính khử
-
B.
tính base
-
C.
tính acid
-
D.
tính oxi hóa
Đáp án : D
Nhóm halogen có 7 electron ở lớp ngoài cùng
=> Có xu hướng nhận thêm 1 electron
Nhóm halogen có 7 electron ở lớp ngoài cùng
=> Có xu hướng nhận thêm 1 electron
=> Tính oxi hóa
Câu 3 :
Trong tự nhiên, nguyên tố fluorine tồn tại phổ biến nhất ở dạng hợp chất là
-
A.
Na3AlF6
-
B.
NaF
-
C.
HF
-
D.
CaF2
Đáp án : D
Nguyên tố fluorine tồn tại phổ biến nhất ở dạng hợp chất là calcium fluoride
Câu 4 :
Ở điều kiện thường, halogen tồn tại ở thể rắn, có màu đen tím là
-
A.
F2
-
B.
Cl2
-
C.
Br2
-
D.
I2
Đáp án : D
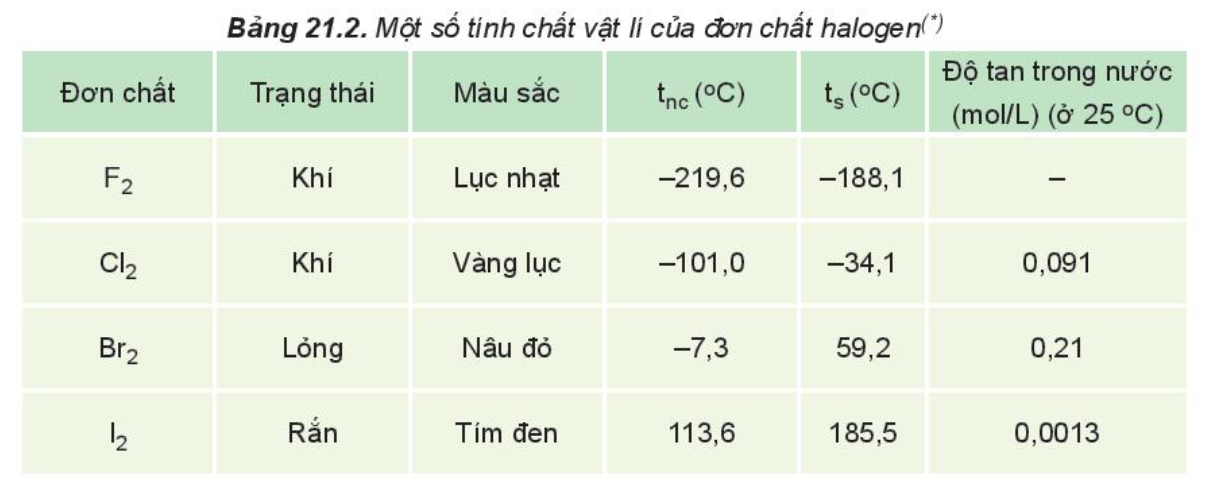
Iodine ở điều kiện thường, tồn tại ở thể rắn, có màu đen tím
Câu 5 :
Đặc điểm nào dưới đây không phải là đặc điểm chung của các nguyên tố halogen (F, Cl, Br, I)?
-
A.
Nguyên tử có khả năng thu thêm 1e.
-
B.
Tạo ra hợp chất liên kết cộng hóa trị có cực với hiđro.
-
C.
Có số oxi hóa -1 trong mọi trường hợp.
-
D.
Lớp electron ngoài cùng của nguyên tử có 7 electron.
Đáp án : C
Trong tất cả các hợp chất F chỉ có số oxi hóa -1 vì F có độ âm điện lớn nhất
Các nguyên tố halogen khác ngoài số oxi hóa -1 còn có các số oxi hóa +1, +3, +5, +7.
Câu 6 :
Đặc điểm nào dưới đây là đặc điểm chung của các đơn chất halogen (F2, Cl2, Br2, I2)?
-
A.
Ở điều kiện thường là các chất khí.
-
B.
Có tính oxi hóa mạnh.
-
C.
Vừa có tính oxi hóa, vừa có tính khử.
-
D.
Tác dụng mạnh với nước.
Đáp án : B
A sai vì ở điều kiện thường F2 và Cl2 là chất khí, Br2 là chất lỏng, I2 là chất lỏng
B đúng
C sai vì F2 chỉ có tính oxi hóa, không có tính khử; Cl2, Br2, I2 vừa có tính oxi hóa, vừa có tính khử
D sai vì F2 tác dụng mạnh với nước; Cl2, Br2, I2 tác dụng với nước khó khăn hơn, cần có xúc tác.
Câu 7 :
Các nguyên tố halogen thuộc nhóm nào trong bảng tuần hoàn
-
A.
VIIIA
-
B.
VIA
-
C.
VIIA
-
D.
IIA
Đáp án : C
Các nguyên tố halogen thuộc nhóm VIIA trong bảng tuần hoàn
Câu 8 :
Trong cơ thể người, nguyên tố iodine tập trung ở tuyến nào sau đây?
-
A.
Tuyến thượng thận
-
B.
Tuyến tụy
-
C.
Tuyến yên
-
D.
Tuyến giáp trạng
Đáp án : D
Trong cơ thể người, nguyên tố iodine tập trung chủ yếu ở tuyến giáp trạng
Câu 9 :
Trong dãy halogen, nguyên tử có độ âm điện nhỏ nhất là
-
A.
fluorine
-
B.
chlorine
-
C.
bromine
-
D.
iodine
Đáp án : D
Trong dãy halogen, độ âm điện giảm dần
=> Iodine có độ âm điện nhỏ nhất
Câu 10 :
Chỉ thị nào sau đây thường dùng để nhận biết dung dịch I2
-
A.
Phenolphtalein
-
B.
Hồ tinh bột
-
C.
Quỳ tím
-
D.
Nước vôi trong
Đáp án : B
Dung dịch iodine tác dụng với hồ tinh bột có hiện tượng: dung dịch từ vàng => xanh tím
Câu 11 :
Phát biểu nào sau đây không đúng khi nói về nguyên tử các nguyên tố nhóm VIIA?
-
A.
Có 7 electron hóa trị.
-
B.
Theo chiều tăng dần của điện tích hạt nhân nguyên tử thì độ âm điện giảm.
-
C.
Theo chiều tăng dần điện tích hạt nhân nguyên tử thì khả năng hút cặp electron liên kết giảm.
-
D.
Theo chiều tăng dần điện tích hạt nhân nguyên tử thì bán kính nguyên tử giảm.
Đáp án : D
- Đáp án: D
- Giải thích: D sai vì trong nhóm VIIA, theo chiều tăng dần điện tích hạt nhân nguyên tử thì bán kính nguyên tử tăng.
Câu 12 :
Nguyên nhân dẫn đến nhiệt độ nóng chảy, nhiệt độ sôi của các đơn chất halogen tăng từ fluorine đến iodine là do từ fluorine đến iodine,
-
A.
khối lượng phân tử và tương tác van der Waals đều tăng.
-
B.
tính phi kim giảm và tương tác van der Waals tăng.
-
C.
khối lượng phân tử tăng và tương tác van der Waals giảm.
-
D.
độ âm điện và tương tác van der Waals đều giảm.
Đáp án : A
- Đáp án: A
Câu 13 :
Phát biểu nào sau đây là không đúng khi nói về đơn chất nhóm VIIA?
-
A.
Tính chất đặc trưng là tính oxi hoá.
-
B.
Màu sắc đậm dần từ fluorine đến iodine.
-
C.
Từ fluorine đến bromine rồi iodine, trạng thái của các đơn chất chuyển từ khí đến lỏng rồi rắn.
-
D.
Khả năng phản ứng với nước tăng từ fluorine đến iodine.
Đáp án : D
- Đáp án: D
- Giải thích: D sai vì khả năng phản ứng với nước giảm từ fluorine đến iodine.
Câu 14 :
Phát biểu nào sau đây là SAI khi nói về tính chất và phản ứng của đơn chất nhóm VIIA?
-
A.
Tính oxi hoá giảm dần từ fluorine đến iodine.
-
B.
Phản ứng với nhiều kim loại, tạo thành hợp chất ion. Phản ứng với một số phi kim, tạo thành hợp chất cộng hoá trị.
-
C.
Khi phản ứng với đơn chất hydrogen, các đơn chất nhóm VIIA thể hiện tính khử.
-
D.
Khi phản ứng với đơn chất hydrogen, mức độ phản ứng giảm dần từ fluorine đến iodine.
Đáp án : C
- Đáp án đúng là: A, B, D
- Giải thích: C sai vì khi phản ứng với đơn chất hydrogen, các đơn chất nhóm VIIA thể hiện tính oxi hóa.
Câu 15 :
Phát biểu nào sau đây là sai khi nói về phản ứng của đơn chất halogen với hydrogen?
-
A.
Các phản ứng đều phát nhiệt mạnh và kèm hiện tượng nổ.
-
B.
Phản ứng giữa fluorine với hydrogen diễn ra mãnh liệt nhất.
-
C.
Điều kiện và mức độ phản ứng phù hợp với xu hướng giảm dần tính oxi hóa từ fluorine đến iodine.
-
D.
Do hợp chất hydrogen iodide sinh ra kém bền (giá trị năng lượng liên kết nhỏ) nên phản ứng giữa iodine với hydrogen là phản ứng hai chiều.
Đáp án : A
- Đáp án: B, C, D
- Giải thích: A sai vì phản ứng giữa H2 và Br2 cần đun nóng, phản ứng diễn ra chậm; phản ứng giữa I2 và H2 cần đun nóng để diễn ra, phản ứng là thuận nghịch.
Câu 16 :
Phát biểu nào sau đây là không đúng khi nói về phản ứng của đơn chất nhóm VIIA với dung dịch muối halide?
-
A.
Bromine phản ứng dễ dàng với dung dịch sodium fluoride để tạo ra đơn chất fluorine.
-
B.
Khi cho vào dung dịch sodium chloride, fluorine sẽ ưu tiên phản ứng với nước.
-
C.
Có thể sục khí chlorine vào dung dịch chứa potassium iodide để thu được iodine.
-
D.
Iodine khó tan trong dung dịch sodium chloride.
Đáp án : A
- Đáp án: A
- Giải thích: A sai vì Bromine không phản ứng với dung dịch sodium fluoride.
Câu 17 :
Phát biểu nào sau đây là không đúng khi nói về một số ứng dụng của đơn chất chlorine?
-
A.
Khí chlorine có thể được dùng để tạo môi trường sát khuẩn cho nguồn nước cấp.
-
B.
Khí chlorine phản ứng với dung dịch sodium hydroxide tạo dung dịch nước Javel dùng để sát khuẩn trong công nghiệp và trong gia đình.
-
C.
Khí chlorine được sử dụng để sản xuất hydrogen chloride, từ đó tạo hydrochloric acid.
-
D.
Do có độc tính, khí chlorine được sử dụng để trừ sâu trong nông nghiệp.
Đáp án : D
- Đáp án: D
- Giải thích: Khí chlorine không được sử dụng để trừ sâu trong nông nghiệp.
Câu 18 :
Ứng dụng nào sau đây không phải của Cl2?
-
A.
Xử lí nước bể bơi.
-
B.
Sát trùng vết thương trong y tế.
-
C.
Sản xuất nhựa PVC.
-
D.
Sản xuất bột tẩy trắng.
Đáp án : B
- Đáp án: B vì đây là ứng dụng của iodine
Câu 19 :
Halogen nào được dùng trong sản xuất nhựa Teflon?
-
A.
Chlorine.
-
B.
Iodine.
-
C.
Fluorine.
-
D.
Bromine.
Đáp án : C
Dựa vào công thức của nhựa Teflon là -(CF2-CF2)-n
- Đáp án: C
Câu 20 :
Nguyên tố halogen được dùng trong sản xuất nhựa PVC là
-
A.
chlorine.
-
B.
bromine.
-
C.
phosphorus.
-
D.
carbon.
Đáp án : A
Dựa vào công thức của nhựa PVC là -(CH2-CH(Cl))-n
- Đáp án: A
Câu 21 :
Halogen được điều chế bằng cách điện phân có màng ngăn dung dịch muối ăn là
-
A.
fluorine.
-
B.
chlorine.
-
C.
bromine.
-
D.
iodine.
Đáp án : B
Dựa vào công thức của muối ăn là NaCl
- Đáp án: B
Luyện tập và củng cố kiến thức Bài 22. Hydrogen halide. Muối halide Hóa 10 với đầy đủ các dạng bài tập trắc nghiệm có đáp án và lời giải chi tiết
Xem chi tiết

